Mycoplasma controle is sleutelfactor in longgezondheid

Primaire en secundaire ziekteverwekkers
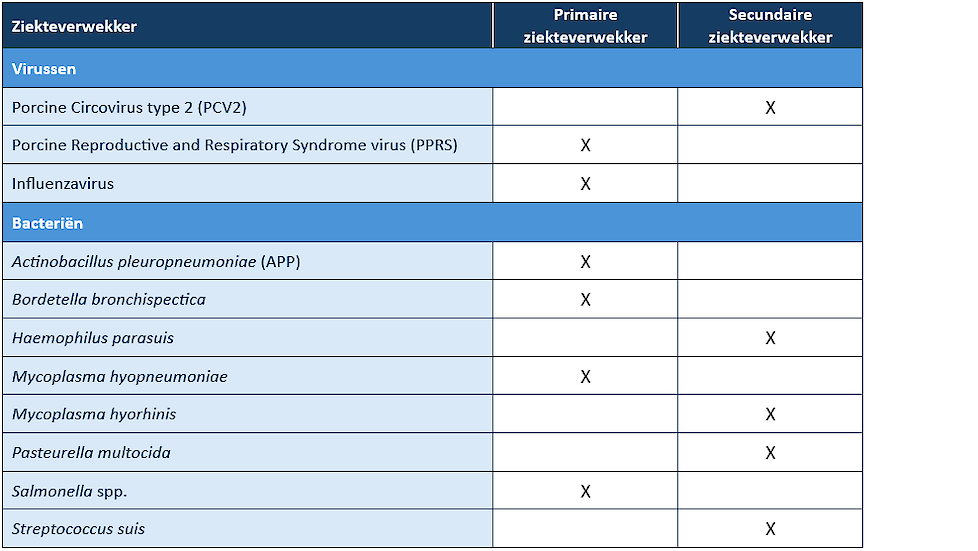
Verschillende virale en bacteriële ziekteverwekkers zijn betrokken bij het PRDC. Sommige kunnen op zichzelf, als gevolg van hun eigen ziekteverwekkend vermogen, luchtwegproblemen veroorzaken. Dit worden primaire ziekteverwekkers genoemd. Andere zullen enkel bij aanwezigheid van andere ziekteverwekkers (zgn. co-infecties) of andere niet-infectieuze factoren (zgn. cofactoren) in staat zijn om luchtwegproblemen te veroorzaken. Dit noemt men secundaire ziekteverwekkers. In onderstaande tabel zijn enkele vaak voorkomende ziekteverwekkers geklasseerd op basis van hun vermogen om op zichzelf of enkel bij aanwezigheid van co-infecties of cofactoren luchtwegproblemen te veroorzaken.
Niet-infectieuze factoren
Verschillende niet-infectieuze factoren spelen een rol bij de ontwikkeling van luchtwegaandoeningen1, door ervoor te zorgen dat ziekteverwekkers zich beter kunnen verspreiden in de varkensstapel, door ongunstige omstandigheden te creëren die zorgen voor verhoogde stress bij de dieren of door directe schade aan de luchtwegen. De niet-infectieuze factoren die bijdragen aan het ziekteproces kunnen worden gedeeld in drie groepen, met name omgeving, management en dierfactoren. Het is bekend dat omgevingsstressoren zoals extreme temperatuurschommelingen, verhoogde luchtvochtigheid of te hoge ammoniakconcentraties varkens vatbaar maken voor luchtwegaandoeningen. Managementfactoren zoals niet all-in/all-out werken en te hoge hokbezetting bevorderen de verspreiding van ziekteverwekkers. Daarnaast zijn de leeftijd en de immuun- en vaccinatiestatus van varkens diergerelateerde factoren die bepalend zijn voor de ziektegevoeligheid van varkens.
Mycoplasma hyopneumoniae verergert de effecten van andere infecties
De invloed van Mycoplasma hyopneumoniae (M.hyo) op het verloop en de ernst van co-infecties werd in verschillende wetenschappelijke studies onderzocht. Zo werd onder andere aangetoond dat M.hyo de schadelijke effecten verergert van infecties met Porcine Circovirus type 2 (PCV2), Actinobacillus pleuropneumoniae (APP) en Porcine Reproductive and Respiratory Syndrome virus (PRRS).
- M.hyo en Circovirus
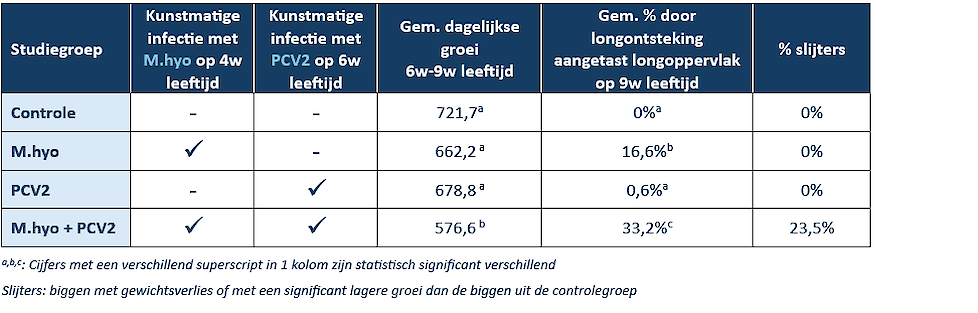
De interactie tussen M.hyo en circovirus (PCV2) infecties werd onderzocht in een laboratoriumstudie.2 In deze studie waren 4 diergroepen betrokken. Een eerste groep biggen werd op 4 weken leeftijd kunstmatig geïnfecteerd met M.hyo. Een tweede groep biggen werd op 6 weken leeftijd kunstmatig geïnfecteerd met PCV2. Een derde groep biggen werd zowel op 4 weken leeftijd met M.hyo als op 6 weken leeftijd met PCV2 geïnfecteerd. Daarnaast was er ook een vierde groep controlebiggen, die niet geïnfecteerd werd met M.hyo of PCV2. De hoeveelheid PCV2 virus in het bloed van de biggen werd wekelijks gemeten, vanaf 6 weken leeftijd. Een deel van de biggen werd geëuthanaseerd op 9 weken leeftijd, de rest van de biggen werd geëuthanaseerd op 11 weken leeftijd. Op dit tijdstip werd de ernst van de PCV2-gerelateerde letsels en de hoeveelheid PCV2 virus in de longen en het lymfeweefsel gemeten. Daarnaast werd ook het percentage longoppervlak dat aangetast was door longontsteking gemeten en werd de dagelijkse groei en het percentage slijters bepaald. Enkele resultaten zijn weergegeven in onderstaande tabel.
Uit deze studie blijkt dat M.hyo de ernst van PCV2-gerelateerde letsels in de longen en lymfeweefsels verhoogt, de hoeveelheid PCV2 virus in bloed en longen verhoogt en duur van de aanwezigheid van PCV2 virus in de longen en lymfeweefsels verlengt. Bovendien verhoogt het de kans op slijters. 2
- M.hyo en APP
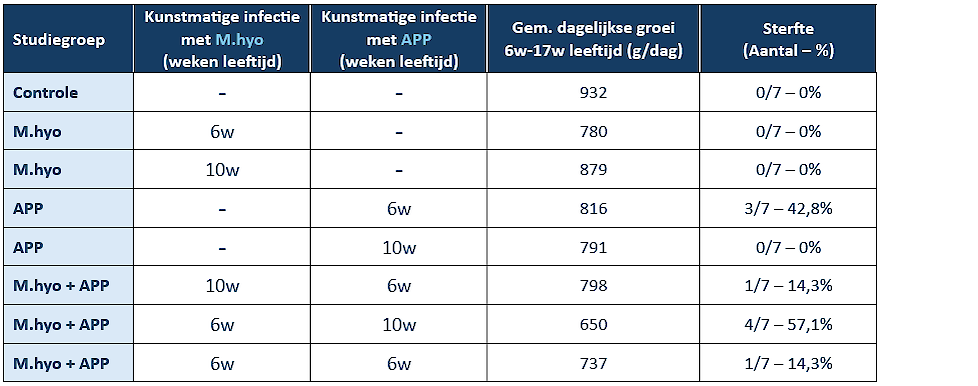
Ook het versterkend effect van M.hyo op een APP-infectie werd bevestigd in een wetenschappelijke studie.3 In deze studie werden twee groepen van elk 7 biggen kunstmatig geïnfecteerd met M.hyo, op 6 weken of 10 weken leeftijd. Verder werden ook twee groepen met 7 biggen geïnfecteerd met APP, op 6 of 10 weken leeftijd. Daarnaast werden er 3 groepen van elk 7 biggen geïnfecteerd met zowel M.hyo als APP. Bij een groep vonden beide infecties tegelijk op 6 weken leeftijd plaats. Bij een andere groep vond eerst een M.hyo infectie plaats op 6 weken leeftijd, gevolgd door een APP infectie op 10 weken leeftijd. Bij nog een andere groep vond eerst een APP infectie plaats op 6 weken leeftijd, gevolgd door een M.hyo infectie op 10 weken leeftijd. Verder werd er ook een controlegroep met 7 biggen in de studie opgenomen, die niet geïnfecteerd werden. De dagelijkse groei van 6 tot 17 weken leeftijd en de sterfte van de verschillende studiegroepen is weergegeven in onderstaande tabel.
De varkens die eerst een M.hyo infectie doormaakten gevolgd door een APP-infectie 4 weken later, waren het zwaarst getroffen. Zij vertoonden zware longletsels en klinische symptomen zoals koorts en hoest. De gemiddelde dagelijkse groei was het laagst in deze groep en bedroeg 650 g/dag. Dit komt overeen met een 282 gram/dag lagere groei dan de niet geïnfecteerde controlegroep die een groei van 932 g/dag noteerde. Bovendien noteerde deze groep ook de hoogste sterfte. Dit wijst erop dat M.hyo de ernst van een APP infectie kan versterken.
- M. hyo en PRRS
Ook de invloed van een M.hyo infectie op de ernst van een PRRS-infectie werd eerder onderzocht.4 In deze studie waren 7 groepen biggen betrokken. Twee groepen biggen werden kunstmatig geïnfecteerd met uitsluitend M.hyo, op 3 of 6 weken leeftijd. Een andere groep biggen werd uitsluitend met PRRS geïnfecteerd op 6 weken leeftijd. Daarnaast werden drie groepen biggen geïnfecteerd met zowel M.hyo als PRRS, bij een groep vonden beide infecties plaats op 6 weken leeftijd, bij een andere groep vond de M.hyo infectie plaats op 3 weken en PRRS-infectie op 6 weken leeftijd, bij nog een andere groep vond de M.hyo infectie plaats op 6 weken en de PRRS-infectie op 4,5 weken leeftijd. Tot slot was er ook een controlegroep, die noch met M.hyo noch met PRRS geïnfecteerd werd.
Varkens die zowel met M. hyo als PRRS geïnfecteerd werden vertoonden ernstigere PRRS-gerelateerde klinische symptomen en de PRRS-gerelateerde longletsels waren ernstiger en bleven langer aanwezig dan bij varkens die enkel met PRRS geïnfecteerd werden. M.hyo versterkte het schadelijke effect van een PRRS-infectie, ongeacht of de M.hyo infectie 3 weken voor, anderhalve week na of tegelijk met de PRRS-infectie plaatsvond.
Conclusie
Uit studies is gebleken dat M.hyo de ernst van de letsels in de luchtwegen veroorzaakt door andere virale of bacteriële ziekteverwekkers zoals PCV2, APP en PRRS versterkt en de duur van deze infecties verlengt. M.hyo kan schade veroorzaken in de luchtwegen en zo varkens meer vatbaar te maken voor andere luchtweginfecties. Daarom is een goede controle van M.hyo op het varkensbedrijf van cruciaal belang om de schadelijke effecten en economische verliezen ten gevolge van luchtwegproblemen te minimaliseren.
Bronnen
- Opriessnig et al. (2011). Polymicrobial respiratory disease in pigs. Animal Health Research Reviews, Volume 12, Issue 2, December 2011, p. 133 – 148.
- Opriessnig et al. (2004). Experimental Reproduction of Postweaning Multisystemic Wasting Syndrome in Pigs by Dual Infection with Mycoplasma hyopneumoniae and Porcine Circovirus Type 2. Veterinary Pathology. 2004;41(6):624-640.
- Marois et al. (2009). Experimental infection of SPF pigs with Actinobacillus pleuropneumoniae serotype 9 alone or in association with Mycoplasma hyopneumoniae. Veterinary Microbiology, 135, 283–291.
- Thacker et al. (1999). Mycoplasma hyopneumoniae potentiation of Porcine Reproductive and Respiratory Syndrome Virus-induced pneumonia. J Clin Microbiol. 1999 Mar;37(3):620-7.